Ремонт ДНК своими руками: руководство для клеток
Как уже неоднократно бывало в последние десятилетия, лауреаты Нобелевской премии по химии 2015 года могли бы получить премию и в области физиологии и медицины. В этому году премия присуждена за исследование репарации ДНК – механизмов устранения повреждений в этой молекуле. Лауреатами стали Томас Линдаль (Tomas Lindahl) шведский ученый, работающий сейчас в Институте Фрэнсиса Крика в Великобритании, американец Пол Модрич (Paul Modrich) из Медицинской школы Университета Дьюка и Азиз Санджар (Aziz Sancar), гражданин Турции и США, который работает в Университете Северной Каролины.
Следует помнить, что в репарации ДНК задействовано большое количество клеточных механизмов, выяснением которых долгие годы занимается много ученых. Например, премия Ласкера в этом году тоже была присуждена за исследования в этой области, но другим ученым: Эвелин Уиткин и Стивену Элледжу. Есть немало и других исследователи, которые внесли свой вклад в понимание этих механизмов.
Способность устранить неполадки в ДНК жизненно важна для клетки. Причем этот ремонт клетка должна производить самостоятельно и непрерывно. Изменения в цепочке ДНК возникают в ней каждый день. Более того, согласно опубликованным в 2000 году данным, повреждение ДНК под воздействием факторов окружающей среды, а также происходящих в клетке процессов обмена веществ происходит с частотой от нескольких сотен до тысячи случаев в час. Может порваться одна или обе цепочки в двойной спирали, может возникнуть соединение цепочек, может оказаться поврежденным какой-то нуклеотид или несколько нуклеотидов. Причин таких поломок множество: ультрафиолетовое излучение, свободные радикалы, радиация, сбои во время удвоение ДНК при делении клетки.
К пониманию этого факта одним из первых пришел Томас Линдаль в начале 1970-х, тогда же он предположил, что раз в молекуле ДНК постоянно накапливаются дефекты, то должны существовать механизмы их устранения. Иначе живые организмы просто не смогут существовать. Линдаль начал искать ферменты, которые ремонтируют ДНК. Он делал это, используя ДНК бактерий. Первый такой фермент Томас Линдаль обнаружил в 1974 году, этот фермент используется для устранения повреждений нуклеотида цитозина. Цитозин – одно из слабых мест в молекуле ДНК, так как он сравнительно легко теряет аминогруппу, что приводит к изменению генетической информации. Если «нормальный» цитозин по принципу комплементарности образует в ДНК связи с гуанином, то поврежденный – с аденином. Если повреждение сохранится, то при следующем делении клетки, когда ДНК реплицируется, закрепится мутация, искажающая «генетический текст». Томас Линдаль сумел идентифицировать фермент, который удаляет поврежденный цитозин из бактериальной ДНК.
Вслед за этим последовали более 30 лет непрерывного поиска «ремонтных ферментов», которым Линдаль занимался сначала в Каролинском медицинском институте в Стокгольме, затем в Великобритании, исследовательском центре Imperial Cancer Research Fund (с 2002 года – Cancer Research UK). В 1986 году он стал директором Clare Hall Laboratory. То, что Томас Линдаль с его постоянным интересом к механизмам репарации ДНК стал работать в исследовательских учреждения, посвященных изучению рака, неслучайно. Сейчас ученые полагают, что от 80 % до 90 % онкологических заболеваний связаны с нарушением механизмов репарации.
В итоге Томас Линдаль сумел обнаружить целый ряд ферментов, которые составляют класс ДНК-гликозилаз. Они распознают наличие в ДНК поврежденных азотистых оснований определенных типов и удаляют их, расщепляя связь этого основания с сахарофосфатным остовом молекулы ДНК. Затем вступают в дело другие ферменты. ДНК-полимераза синтезирует соответствующий участок цепочки ДНК вместо удаленного, а ДНК-лигаза сшивает цепочку. Данный вид ремонта ДНК получил название эксцизионная репарация (excision repair) от английского excision «вырезание». В 1996 году Томас Линдаль сумел воспроизвести в лаборатории процесс репарации ДНК человека.
С механизмом эксцизионной репарации связаны исследования Азиза Санджара. В 1970-х годах Санджар заметил любопытное явление: бактерии, получившие смертельную дозу ультрафиолетового излучения, выживают, если их осветить синим светом. Выяснение биохимической природы этого чудесного спасения бактерий стало предметом исследований Санджара в Техасском университете. В 1976 году он сумел клонировать ген, который отвечает за синтез фермента фотолиазы, восстанавливающего повреждения ДНК, нанесенные ультрафиолетом. Также Санджар сумел получить бактерий, которые усиленно продуцировали этот фермент. Как выяснилось, ДНК-фотолиаза действительно активируется видимым светом и использует для работы его энергию.
Репарация ДНК после повреждения ультрафиолетом — образец эксцизионной репарации
Увы, докторская диссертация Санджара, посвященная фотолиазе, тогда не вызвала особого интереса, и три его заявки на должность исследователя в разных университетах были отклонены. Тогда Азиз Санджар стал работать лаборантом в Медицинской школе Йельского университета. Там он смог продолжить свои работы по изучению того, как ДНК бактерий восстанавливается после ультрафиолетового облучения. Санджар и его коллеги поняли, что у бактерий есть две системы восстановления. Одна работает на свету (она основана на фотолиазе), а другая действует и в темноте. За несколько лет работы Санджар смог определить бактериальные ферменты, кодируемые тремя генами uvrA, uvrB и uvrC. Он экспериментально показал, как эти ферменты идентифицируют поврежденный участок ДНК, а затем делают два разреза в цепочке, удаляя кусок из 12-13 нуклеотидов, содержащий поврежденную часть. Затем в дело вступают уже упоминавшиеся ДНК-полимераза и ДНК-лигаза, достраивая недостающий фрагмент и сшивая цепочку.
После публикации своей работу в 1983 году Азиз Санджар был приглашен в Университет Северной Каролины, где продолжил исследования механизмов репарации. Параллельно с работами Томаса Линдаля он перешел от бактериальной ДНК к ДНК человека. Как оказалось, там функционируют пусть несколько более сложные, но в целом сходные механизмы. Специфический фермент определяет тот тип повреждения ДНК, за который он отвечает. Поврежденный участок вырезается, синтезируется участок на замену, затем разрезы зашиваются.
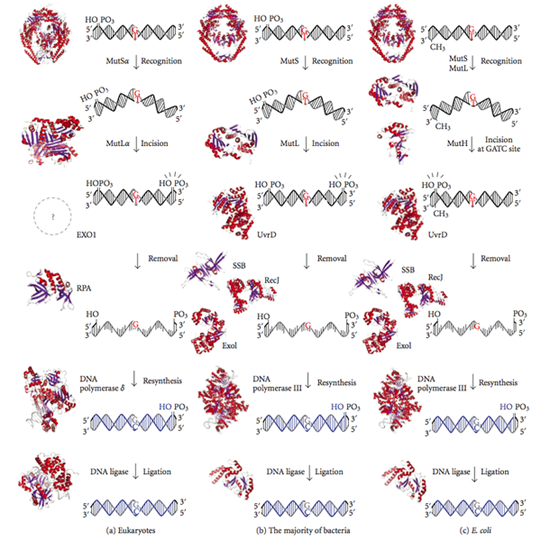
Третий лауреат, Пол Модрич, в начале своей карьеры исследовал ДНК-полимеразы и ДНК-лигазы, а в дальнейшем обратил внимание на другой класс ферментов, задействованных в репарации ДНК. Работа этих ферментов, получивших название ДНК-метилтрансферазы, заключается в присоединении метильной группы (CH3-) к цепочки ДНК. Как установил Пол Модрич, эти метильные группы могут служить указателями, помогающими другим ферментам разрезать цепочку ДНК в нужном месте. В дальнейних исследованиях Пол Модрич совместно с молекулярным биологом Мэтью Мезельсоном (Matthew Meselson) открыл особый механизм репарации ДНК – репарацию ошибочно спаренных нуклеотидов (DNA mismatch repair). Она требуется, когда в процессе удвоения ДНК при клеточном делении возникают неправильные пары нуклеотидов, например, аденин может соединиться с цитозином, а не с тимином. В этом случае клетке важно заменить именно ошибочно возникший нуклеотид, а не его напарника на соседней цепочке, который стоит на своем месте. Как установили ученые, здесь также используется метилирование ДНК. У большинства бактерий ошибочные нуклеотиды, как правило, содержатся на одной из двух цепочек ДНК – дочерней, которая была только что достроена. При этом исходная цепочка содержит присоединенные к ней метильные группы, а дочерняя пока неметилирована. Поэтому ее можно отличить, а дальше использовать уже известный механизм: вырезать, заменить, сшить.
Репарация ошибочно спаренных нуклеотидов у эукариот, большинства бактерий и у бактерии E. coli
Подробное исследование этого механизма заняло у Пола Модрича десять лет. В 1989 году он опубликовал статью, где было показано и подтверждено экспериментами, какие ферменты участвуют в исправлении ошибочно спаренных нуклеотидов.
Помимо описанных систем за последние годы открыты и другие способы репарации ДНК, используемые в живых клетках. Установлена связь нарушений в работе систем ремонта ДНК со многими формами рака. Как выяснили ученые, часто плохая работа систем репарции играет на руку раковым клеткам: они начинают значительно чаще мутировать, и по этой причине могут стать устойчивыми к химиотерапии. Но биологи научились использовать этот механизм и при разработке новых лекарств от рака. Если им удается подавить оставшиеся у раковых клеток механизмы репарации, это приводит к замедлению или полной остановке роста опухоли. Примеров такого лекарства – Olaparib, который ингибирует один из ферментов, задействованных в репарации ДНК.
Источник
Нобелевскую премию по химии дали за механизмы ремонта ДНК
У всех живых организмов ДНК требует постоянного ремонта, и для этой цели в клетках есть несколько главных ремонтных систем, помогающих поддерживать геном в целости и сохранности.
Как мы все хорошо знаем, наша наследственная информация – да и не только наша, а вообще любого живого организма на Земле – хранится в молекулах ДНК. Чтобы эта информация «заработала», её нужно превратить в белок, для чего сначала с какого-то гена, который представляет собой участок ДНК, снимается РНК-копия (происходит транскрипция), а потом на РНК синтезируется молекула белка (трансляция). По сути, в ДНК записаны схемы сборки белковых молекул и дополнительные регуляторные «параграфы», с помощью которых можно очень точно регулировать количество того или иного белка. Кроме того, генетическую информацию нужно также передавать в следующие поколения. Здесь существует специальный молекулярный процесс, репликация, то есть удвоение молекулы ДНК, чтобы одна копия генома смогла перейти дочерней клетке.
Как легко догадаться, сохранность генов стала первейшей задачей, которую пришлось решать живым организмам уже на самых начальных этапах эволюции. Действительно, представим, что в ген прокралась ошибка: в таком случае появляется вероятность, что белок, синтезированный в соответствии с изменённой инструкцией, будет работать не так, как надо, и что испорченный вариант гена перейдёт в следующие поколения. Чтобы этого не происходило, существуют специальные молекулярные машины, выполняющие репарацию ДНК, и именно за описание разных механизмов репарации и была присуждена очередная Нобелевская премия по химии.
Чтобы понять, какие повреждения возможны в ДНК и как их следует исправлять, нужно хотя бы бегло вспомнить химическое строение нуклеиновых кислот. И ДНК, и РНК состоят из множества мономеров-нуклеотидов; нуклеотид же, в свою очередь, состоит из трёх частей: остатка фосфорной кислоты, углевода и азотистого основания. Углевод (рибоза или дезоксирибоза) и фосфорная кислота складываются в сахарофосфатный остов, утыканный азотистыми основаниями, которые как раз выполняют функцию букв генетического кода: А – основание аденин, Т – основание тимин (в РНК вместо тимина – U, урацил), G – основание гуанин, С – основание цитозин. ДНК сложена из двух цепей, объединённых в спираль, и основания на одной цепочке взаимодействуют с другой: аденин – с тимином, гуанин – с цитозином. Это называется правилом комплементарности, благодаря которому клетка может на одной цепи ДНК сделать новую – просто подбирая соответствующие комплементарные нуклеотиды.
Узор оснований в ДНК позволяет зашифровать строение любого белка (подробно организацию генетического кода мы сейчас обсуждать не будем). Так что в интересах «генетической безопасности» буквы ни в коем случае не должны меняться, исчезать, и т. д. А между тем именно так и происходит: в геноме какие-то нуклеотиды постоянно вылетают со своего места, или же меняются на другие, или же в ряду нуклеотидов появляется кто-то лишний. Такие события называются мутациями, и случаются они не только под влиянием внешних факторов, например, радиоактивного или ультрафиолетового излучения. В самой клетке в ходе метаболизма появляются агрессивные молекулы, способные внести мутацию в ДНК. Наконец, реплицирующие машины, удваивающие генетический материал, синтезируют новые цепи всё-таки не со стопроцентной точностью. Замена или выпадение нуклеотида не обязательно приводят к серьезным последствиям, но многие мутации могут запустить рак, или стать причиной какого-нибудь психоневрологического заболевания, или же вывести из строя обмен веществ, и т. д.
Задача систем репарации – искать такие ошибки и своевременно их исправлять. Томас Линдаль (Tomas Lindahl), один из нынешних лауреатов, в 1974 году опубликовал статью, в которой описывал бактериальный фермент, позволяющий восстановить повреждённый цитозин в ДНК. Цитозин (С) склонен терять одну химическую группу, превращаясь в урацил (U), так что в результате предпочтительным напарником в соседней цепочке ДНК для него становится не гуанин (G), а аденин (А). И специальный белок у бактерий занимается тем, что вырезает из ДНК поломанный цитозин, ликвидируя мутацию.
Несколько десятков лет Линдаль занимался тем, что уточнял молекулярный механизм, который был назван эксцизионной (то есть выщепляющей) репарацией оснований. Он есть не только у бактерий, но и у других организмов, вплоть до человека; ключевыми же белками здесь являются ферменты-гликозилазы. Вышеприведённый пример с цитозином – лишь один из возможных, дефектными могут становиться и другие «буквы»-основания. Ремонт же начинается с того, что ДНК-гликозилаза отщепляет повреждённую «букву». Затем подключаются другие белки, удаляющие из цепи ДНК сахар и фосфорную кислоту, которые держали на себе модифицированное основание. В результате в ДНК-цепочке получается дыра, которую заделывают новые белки: они вставляют в освободившееся место ту «букву», которая тут должна быть.
Но такое точечное вырезание оснований – лишь один из механизмов ремонта ДНК. Ещё в конце 40-х годов прошлого века биологи описали любопытный феномен: бактерии, облучённые ультрафиолетом (или жёстким ионизирующим излучением), переставали расти и гибли, но возвращались к росту, если их освещали обычным светом. Было установлено, что ультрафиолет плохо действует на ДНК, сшивая вместе некоторые пары оснований, сидящие рядом на одной цепи, – такие димеры сильно затрудняли репликацию ДНК. Сам собой напрашивался вывод, что существует какой-то фотоактивируемый белок, который устраняет подобные нуклеотидные аномалии. Азиз Санджар (Aziz Sancar), биохимик из Турции, начал свою научную карьеру в США с того, что успешно определил этот белок (его назвали ДНК-фотолиазой). Однако его результаты в то время мало кого впечатлили. (Впоследствии оказалось, что фотолиаза выполняет едва ли не самую простую ДНК-репарацию: она с помощью энергии света просто разделяет соединённые нуклеотиды. Такой способ ремонта ДНК есть у бактерий, архей, дрожжей, насекомых, но у человека, как и у многих высших эукариот, ничего такого нет.)
Скоро стало ясно, что у бактерий, кроме световой репарации (или фотореактивации), есть ещё и «темновая», которая идёт сама по себе, безо всякого светового стимулирования. В составе исследовательской группы, которая пыталась расшифровать механизм такой репарации, Санджару в течение несколько лет поставил ряд экспериментов, в ходе которых удалось определить ферменты, отвечающие за ремонт ДНК при повреждении ультрафиолетом, и понять механизм их работы. В данном случае из цепи ДНК вырезается не один-единственный повреждённый нуклеотид, а целый кусок, фрагмент из нескольких «букв» (у бактерий – 12-13, у человека – 27-29), содержащий повреждённый участок. Ферменты, которые это делают, называются эксцизионные нуклеазы. Затем наступает очередь другого белка, который делает «заплатку» на то место, откуда вырезали кусочек генетического текста; правильным шаблоном служит другая цепь ДНК (не забываем про принцип комплементарности!). Наконец, последний этап – готовая заплатка с обоих концов с помощью новых ферментов пришивается на «продырявленное» место.
Такую репарацию назвали эксцизионной репарацией нуклеотидов, и поначалу её изучали на бактериях. Что до человека, то у нас всё происходит сложнее, и белков участвует больше, но сам принцип работы у всех организмов тут одинаков: с запасом вырезать повреждённый кусок и сделать его заново. Получается, что с учётом фотолиазы на счету Санджара целых два репарирующих механизма. Необходимо отметить, что, в отличие от «механизма Линдаля» (эксцизионной репарации оснований), которая ремонтирует лишь некоторые разновидности повреждений ДНК, «механизм Санджара» удаляет все возможные повреждения, хотя и с разной эффективностью, и его роль в поддержании стабильности генома весьма и весьма велика.
Наконец, с именем третьего нобелеата, Пола Модрича (Paul Modrich), связано открытие ещё одного механизма ремонта ДНК. Он начинал с исследований ферментов ДНК-метилтрансфераз (или ДНК-метилаз) у бактерий. Их функция состоит в том, чтобы метильными группами метить основания в бактериальной ДНК – если потом в клетку проникнет вирус, то его ДНК будет уничтожена как не имеющая защитных метильных меток. Однако в связи с метилазами обнаружился ещё один странный молекулярный феномен: когда в бактериальную клетку запускали специально сконструированный вирус, в ДНК которого некоторые основания были некомплементарны друг другу, то такие неправильные пары исправлялись как раз с помощью метилазы. Тогда же было выдвинуто предположение, что это нужно при ошибках копирования: хотя, как мы упоминали выше, репликационные машины, удваивающие ДНК, работают очень точно, ошибки у них всё же случаются, и бывает, что напротив генетической «буквы» в одной цепи встаёт совсем некомплементарная ей «буква» в новой цепи. Для устранения таких погрешностей как раз и существует отдельная система, которая называется репарацией ошибочно спаренных нуклеотидов, или мисматч (mismatch)-репарацией, если использовать кальку с английского термина. Метилирование же нужно для того, чтобы обозначать правильную, старую цепь ДНК – ошибка будет исправлена в соответствии с её нуклеотидной последовательностью.
К концу 80-х годов прошлого века Полу Модричу удалось определить все ферменты, участвующие в мисматч-репарации, и даже продемонстрировать их работу в искусственной системе. Вкратце её этапы таковы: специальный белок находит неправильно спаренные нуклеотиды, после чего к нему присоединяется его «коллега», который определяет, на какой цепи находится метильная группа. Затем в дело включаются ферменты, вырезающие из новой (то есть лишённой метильной метки) цепи ДНК фрагмент с неправильной «буквой», после чего ДНК здесь синтезируется заново. Как и в предыдущих случаях, исследователи подтвердили, что такой же механизм работает не только у бактерий, но и у других организмов, вплоть до человека.
Среди систем репарации ДНК есть ещё некоторые разновидности и модификации, не исключено, что в будущем к ним добавятся и другие. Однако три вышеописанных механизма можно назвать основными, присутствующими у большинства живых организмов. Когда речь идёт об исследованиях таких фундаментальных процессов, то известия о Нобелевской премии воспринимаются с некоторым удивлением – кажется, что за это уже давно всё всем дали. Заметим, впрочем, что сама по себе мысль, что у клеток должен быть механизм ремонта ДНК, относительно проста (хотя, по словам Томаса Линдаля, некоторое время назад все были убеждены в исключительной стабильности клеточной ДНК, для которой ремонт-то почти и не нужен). Совсем другое дело – расшифровка механизмов молекулярных процессов, детализация, определение этапов и проч.; собственно, именно на расшифровку механизмов, на подтверждение первоначальной догадки во всех трёх случаях ушли годы исследовательской работы, а потом должны были пройти ещё годы для того, чтобы стало окончательно ясно, что всё именно так, как мы выяснили. И потому в формулировке Нобелевского комитета говорится именно о «механизмах репарации ДНК».
Что же до «народнохозяйственной пользы», то здесь всё просто: ДНК в наших клетках ломается постоянно, и, если её вовремя не ремонтировать, наш геном погрузится в хаос, со всеми вытекающими последствиями. Об этом вполне наглядно говорит статистика: считается, что от 80 % до 90 % всех раковых заболеваний связаны с неправильной работой ДНК-репарирующих систем.
И последнее – мы почти ничего не сказали о том, к каким странам принадлежат новые лауреаты, в каком университете они выполнили свои эпохальные работы и т. д. Однако современная наука, и в особенности такие её области, как молекулярная биология, такова, что вопрос о «национальной принадлежности» того или иного открытия просто бессмыслен. Судите сами: Азиз Санджар родился и получил медицинское образование в Турции, но потом перебрался в Техасский университет в Далласе, где занимался фотолиазой, затем работал в Йеле, а свои нобелевские результаты получил в Университете Северной Каролины в Чапел-Хилл; сейчас он сохраняет двойное гражданство Турции и США. Томас Линдаль родился в Швеции и получил высшее образование в Каролинском институте, затем некоторое время работал в США, а потом переехал в Великобританию, где в Имперском фонде по исследованию рака продолжил ранее начатую работу по расшифровке эксцизионной репарации оснований. С Полом Модричем всё немного проще: он и родился в США, и выучился там, и работал, но опять же его научный путь связан с целым рядом университетов, от Стэнфордского до Университета Дьюка. Иными словами, наукой стоит заниматься там, где вы сможете найти ответы на свои вопросы, и где вы сможете получить результаты, которые принесут пользу всем людям.
Источник